Tämä kirjoitus on toinen osa matala-asteista tulehdusta ja ruokavaliota koskeva kirjoitussarjassani. Edellisessä kirjoituksessa käsittelin sitä, miten tulehdusta mitataan, ja kirjoitin lyhyesti unen, stressin, liikunnan ja laihtumisen vaikutuksesta matala-asteiseen tulehdukseen.
Tässä kirjoituksessa käsittelen rasvoja. Ja kuten useimmiten ennenkin, en käy läpi koe-eläintuloksia, vaan pelkästään ihmistutkimuksia.
Biokemia ja tausta
Omega-6 rasvahapoista linolihappo (LA) on ihmisille välttämätön, ja sitä saadaan lähinnä vain kasviöljyistä, joskin esim. sianrasva sisältää pieniä määriä linolihappoa (rasvainen liha lienee ollut ennen muinoin Suomessa linolihapon harvoja lähteitä). Toinen merkittävä omega-6 rasvahappo on arakidonihappo (AA)
Omega-3 rasvahapoista α-linoleenihappo (ALA) on myös välttämätön. Sen lähteitä ovat myös pääasiallisesti kasviöljyt, pähkinät ja siemenet. Omega-3 rasvahapoista merkittäviä ovat erityisesti DHA ja EPA, joita saadaan erityisesti rasvaisesta kalasta.
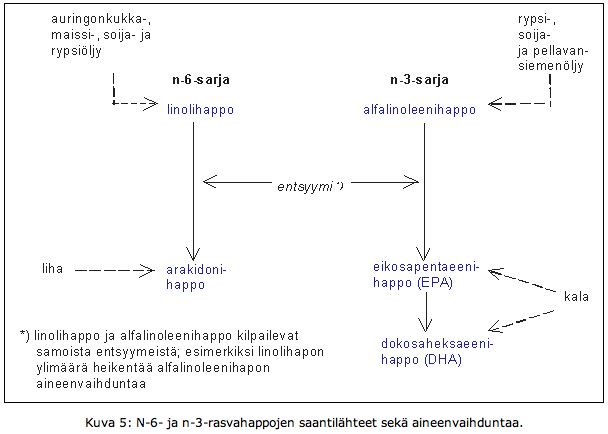
Perinteinen oppi näiden rasvojen aineenvaihdunnasta menee kutakuinkin Helsingin yliopiston verkkokurssilla esitetyn mukaisesti (kuva).
Arakidonihaposta, DHA:sta ja EPA:sta muodostuu elimistössä eikosanoideja, kuten leukotrieenejä, tromboksaania ja prostaglandiinia. Nämä eikosanoidit puolestaan osallistuvat tulehdusreaktioiden syntyyn, joko hillitsemällä sitä tai lisäämällä sitä.
Tässä avoimen yliopiston tekstissä ei oteta kantaa yksioikoisesti kantaa siihen onko syntyvä arakidonihappo tulehdusta lisäävää vai ei. Teksti toteaa:
”N-6-sarjan arakidonihaposta muodostuvat eikosanoidit ovat tilanteen mukaan joko edullisia tai epäedullisia, kun taas n-3-sarjan EPA:sta rakentuneet eikosanoidit ovat joko edullisia tai neutraaleja.”
Näin on ravitsemustieteilijää kai ainakin periaatteessa opetettu pidempään.
Viime aikoina kuitenkin on härkäpäisesti jyrätty näkemystä, jonka mukaan omega-3 rasvahapot ovat tulehdusta lievittäviä ja omega-6 rasvahapot tulehdusta kiihdyttäviä. Sivussa esimerkiksi blogosfäärikeskusteluissa on ollut tyydyttyneenn rasvan rooli, vaikkakin tieteentekijät ja asiantuntijat sitä ovatkin pitäneet esillä jossain määrin esillä (Chair&Kim 2010).
Ehkäpä kaikkein jyrkimmin omega-6 rasvahappoihin on suhtautunut Suomessa Antti Heikkilä. Monet muut kuten esimerkiksi rasvakirjan kirjoittanut Sompin pariskunta ovat olleet samaa mieltä. Monet suomalaisten seuraamat jenkkibloggaajat ovat olleet varsinkin paleo-piireissä samoilla linjoilla. Heikkilä toteaa räväkkään tyyliinsä blogissaan ”Miksi en käytä rypsiöljyä”
”Kun puhutaan hyvistä ja huonoista rasvoista, todellinen pahis on arakidonihappo (AA). Elimistö valmistaa itse arakinodihappoa linolihaposta, jotka molemmat ovat omega-6-rasvoja. Elimistö tarvitsee näitä rasvoja, mutta liika on haitallista. … Arakidonihappo on erittäin välttämätön rasva, mutta erittäin myrkyllinen, jos sitä on liikaa. Siksi arakidonihapon pitoisuuden säätely on olennaisen tärkeää elimistölle. Arakidonihappo tappaa koe-eläimet suonensisäisesti ruiskutettuna, kun taas muilla rasvoilla ja kolesterolilla ei ole mitään vastaavaa vaikutusta.”
Heikkilän teoria rypsiöljyn vaarallisuudesta perustuu siihen, että linolihaposta syntyy arakidonihappoa liikaa, joka myrkyttää elimistön. Hän tarjoaa myös muita selityksiä, mutta edellä lainattu on se tärkein. Tämän saman ajatuksen on niellyt sellaisenaan erittäin moni englanninkielisen blogosfäärin kärjessä kulkeva henkilö, sekä varsin useat merkittävät tieteen tekijätkin, kuten esim. Lyon Diet Heart -tutkimuksesta kuuluisa Michael de Lorgeril.
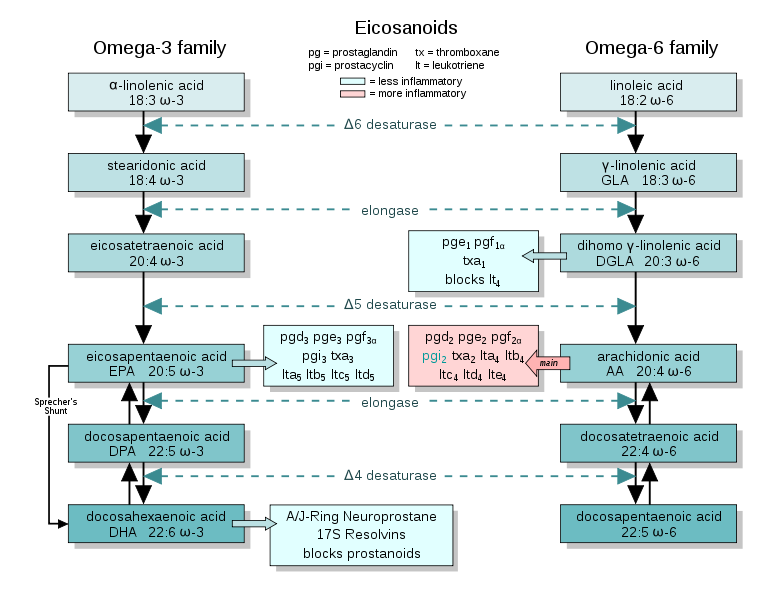
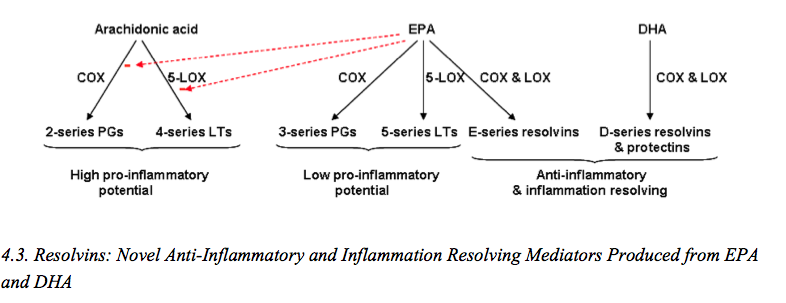
Oheinen kuva Wikipediasta kertoo perusajatuksen, joka on periaatteessa laajasti hyväksytty. Punaisessa laatikossa esitetyt arakidonihapon aineenvaihduntatuotteet lisäävät tulehdusta, kun taas vihreässä laatikossa esitetyt EPA:n aineenvaihduntatuotteet vähentävät tulehdusta.
Tämä ajattelu (kuva yllä) on ohjannut tyystin ajatusta eri rasvojen vaikutuksesta tulehdukseen. On jäänyt tyystin taka-alalle seuraavat kysymykset:
- Mikä on tyydyttyneen rasvan merkitys tulehdukselle?
- Mikä kertatyydyttymättömän rasvan, kuten oliiviöljyn vaikutus tulehdukselle?
- Mikä on rasvan kokonaissaannin vaikutus tulehdukselle?
- Mikä on ruokavalion lihasta saatavan arakidonihapon saannin vaikutus tulehdukselle (ei siis pelkästään linolihapon)?
Kaikki eivät toki ole nielleet mukisematta edellä kuvattua hyvä-paha -astelmaa. Esimerkiksi Harvardin professori Walter Willett toteaa, että n-6/n-3 suhde ei ole tarpeellinen.
”Adequate intakes of both n-6 and n-3 fatty acids are essential for good health and low rates of cardiovascular disease and type 2 diabetes, but the ratio of these fatty acids is not useful. Reductions of linoleic acid to ”improve” this ratio would likely increase rates of cardiovascular disease and diabetes.” (Willett 2007)
Suomessa Willettin kanssa samoilla linjoilla on mielestäni ollut esimerkiksi emeritusprofessori Antti Aro. Hänhän on esimerkiksi puolustanut P/S -suhteen uudelleen käyttöön ottoa (P/S -suhde painottaa linolihappoa). Myös muut ravitsemustieteen professorit ja dosentit ovat olleet enemmän Willettin linjoilla kun blogosfäärin vahvimpien äänenpainojen linjoilla.
Rasvan määrä
Ennen kuin mennään arakidonihapon ja kalaöljyn maailman muutama sana rasvan määrästä sinänsä. Ruokavalion rasvan määrällä näyttää olevan vaikutusta tulehduksen syntyyn.

Kermasta on tullut rasvarasituksen vakioaine, aivan kuten glukoosiliuoksesta sokerirasituksen. Yli 50 gramman kerma-annos lisää useita tulehdusmarkkereita.
LPS, lipopolysakkaridi (endotoksiini)
Rasva lisää ihmisillä, koe-eläintutkimuksien kanssa samansuuntaisesti, suolistobakteerien tuottaman LPS:n imeytymistä ja siten pitoisuutta veressä. Kuten edellisessä kirjoituksessa käsittelin, LPS on endotoksiini, joka aiheuttaa laajalti tulehdusta elimistössä. Se myös lisää suoliston läpäisevyyttä, eli aiheuttaa vuotava suoli -ilmiötä.
1) Ranskalaisessa poikkileikkaustutkimuksessa havaittiin, että rasvan runsas saanti ruokavaliosta lisää LPS:n määrää veressä. Koska tutkimus on luonteeltaan poikkileikkaus, ei sillä voida osoittaa syy-yhteyttä. (Amart et al. 2008)
2) Sairaaloisen lihavilla tehdyssä avoimessa tutkimuksessa (N=40) havaittiin, että 50 grammaa rasvaa aiheuttaa merkittävän plasman ja kylomikronien LPS-pitoisuuden nousun. Nousu oli melko pieni niillä, joilla vähiten insuliiniresistenssiä ja alhaisimmat triglyseridit. LPS:n lisääntyminen oli suurta niillä, jotka vahva insuliiniresistenssiä ja korkeat triglyseridit. Kyseessä oli ainoastaan aterianjälkeisten arvojen mittaus, eikä verrokkiryhmää ollut. (Clemente-Postigo et al. 2012)
3) Tyypin 2 diabetikoilla, esidiabeetikoilla ja terveillä toteutettiin satunaistettu tutkimus, jossa seurattiin aterianjälkeisiä LPS-arvoja. 75 gramman annos rasvaa (ja 6 g proteiinia ja 5 g hh) lisäsi merkittävästi LPS-pitoisuuksia 4 tuntia ateriasta. Kaikkein selvin LPS:n nousu oli diabeetikoilla (kuva alla), Harte et al. 2012

Plasman LPS eli endotoksiinivaste 75 rasva-annoksen jälkeen. Lähde: Harte et al. Diabetes Care 35:375–382, 2012
Kiinnostava sivujuonne on mainittava. LPS poistuu elimistöstä HDL-kolesterolin vaikutuksesta (!). Lisäksi korkeat LPS-pitoisuudet korreloivat diabeteksen puhkeamisen kanssa. (Pussinen et al. 2011). HDL-kolesterolin määrä näyttäisi olevankin käänteisessä yhteydessä LPS-määrää veressä (Harte et al. 2008)
Useamman viikon mittaisia tutkimuksia ei ilmeisesti vielä ole, vaan edellä esitellyt aterianjälkeistä tilaa kuvaavat tutkimukset ovat ainoita lajissaan. Huomioitavaa on myös, että kyse on kerta-annoksista. Sopeutuuko elimistö esimerkiksi runsaaseen rasvan saantiin vähentäen LPS:n imeytymistä ajan funktiona, ei selviä näistä tutkimuksista. On huomitava, että pienin käytetty rasva-annos on ollut 50 grammaa ja tutkimuksissa on käytetty vain kermaa.
Ei ole siis tietoa, lisääkö kasviöljyt LPS:n imeytymistä.
CRP ja muut tulehdusmarkkerit
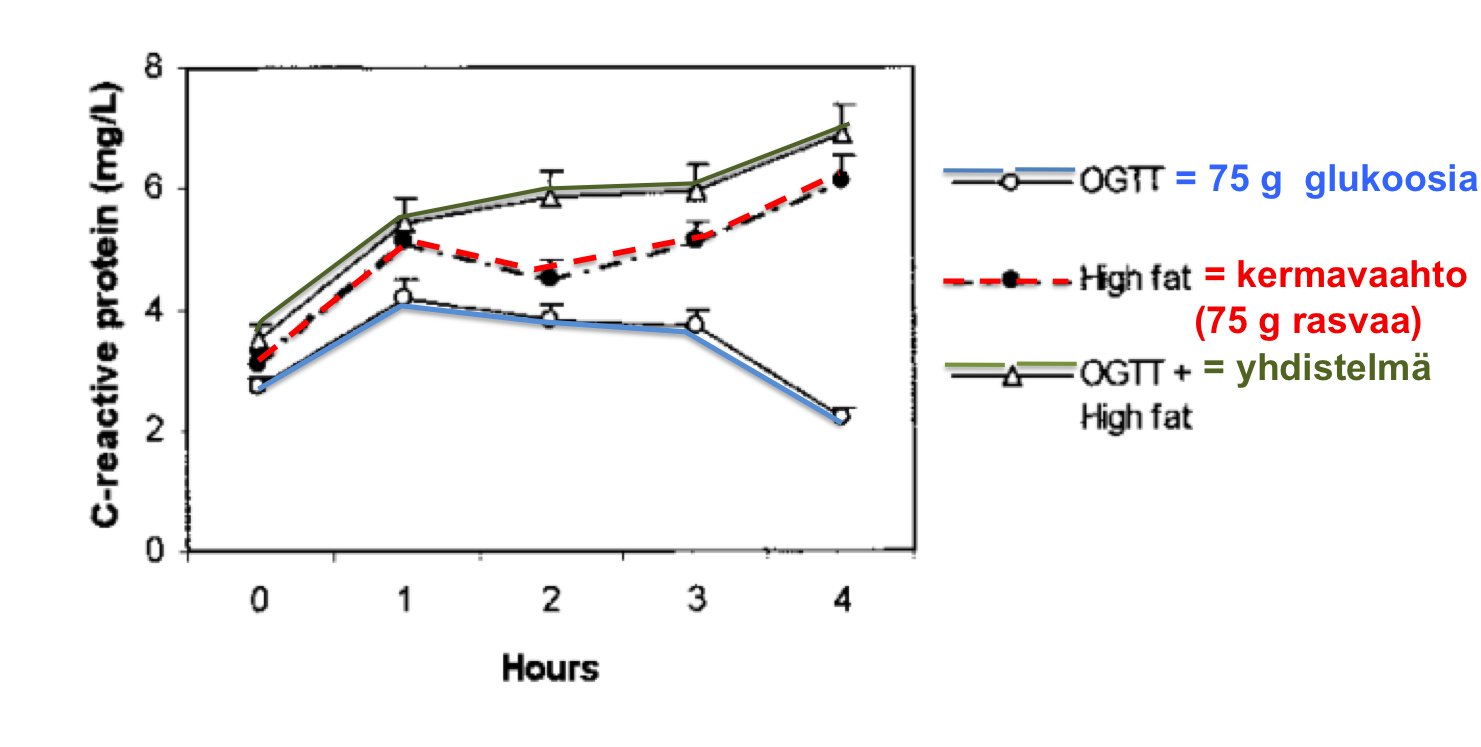
1) Olen jo aiemmin esitellyt tutkimuksen, jonka mukaan 75 grammaa rasvaa kerta-annoksen lisää CRP-arvoja merkittävästi (Ceriello et al. 2005). Tässä kuvassa on ennenaikojaan myös glukoosi, sillä kirjoian hiilihydraattien vaikutuksesta myöhemmin, mutta olkoon.
Runsasrasvainen ateria
Koska rasvaa syödään harvoin itsessään, vaikkapa kermana, tällaisia määriä, vaan kyse on jonkinlaisesta ateriasta, otan esimerkiksi yhden tutkimuksen runsasrasvaisesta ateriasta. Tässä tutkimuksessa koehenkilöt (n=36, miehiä) nauttivat kananmunaa, maitoa, persikkaa, leipää ja maapähkinävoita sekä kermaa sisältäneen aterian. Aterian energiasta 64 % tuli rasvasta. Ateria oli erittäin suuri, siinä oli energiaa n. 2000 kcal. Ainoastaan IL-6 arvo nousi koeaterian seurauksena, kun taas TNF-α väheni 4 tunnin kohdalla. CRP:ssä ei havaittu muutoksia. Tutkimus osoittaa, että todellisen aterian vasteet saattavat olla hyvin erilaisia kuin isoloitujen rasvarasituksien tulokset. Blackburn et al. 2006
Nappo et al. 2002. Tässä tutkimuksessa verrattiin runsasrasvaisen aterian (englantilaistyyppinen aamiainen) ja hiilaripitoisen vähärasvaisen aterian (juustoton pitsa) tulehdusvasteita tyypin 2 diabeetikoilla ja terveillä (n=20). Lisäksi edellämainittujen aterioiden vaikutuksia testattiin C/E-vitamiinivalmisteen kanssa ja ilman. Terveillä henkilöillä pizza ei aiheuttanut tulehdusvasteita, mutta diabeetikoilla aiheutti useilla mittareilla selvän vasteen. Sen sijaan runsasrasvainen ateria, jossa oli rasvaa (58 E %) ja myös hiilihydraatteja (28 E %), aiheutti sekä terveillä että tyypin 2 diabeetikoilla selvän tulehdusvasteen. Terveiden tulehdusvaste saatiin ehkäistyä sillä, että he ottivat vitamiinivalmisteen, kun taas diabeetikoilla vitamiinivalmiste ei estänyt rasvaisen aterian aiheuttamaa tulehdusvastetta. Runsasrasvainen ateria näytti siis aiheuttavan pahemman tulehdusvasteen, ja terveillä tämän tulehdusvasteen saattoi estää C/E-vitamiinivalmisteella, mutta diabeetikoilla ei. Mielestäni tärkeää on huomata, että koeruuassa muuttui myös muut komponentit kuin rasva (kuitu, tomaatin määrä, jne.)
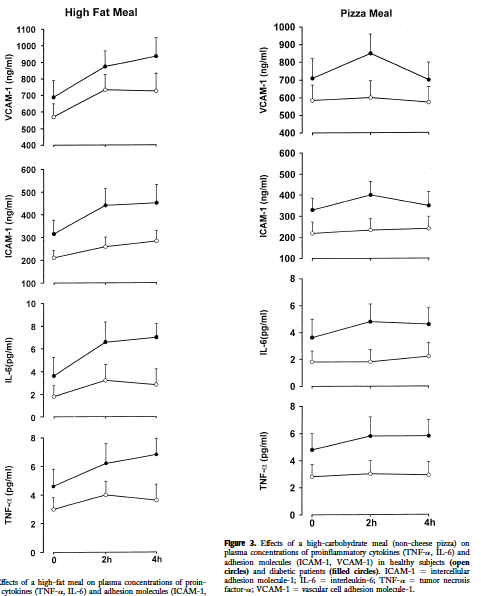
Runsas- ja vähärasvaisten aterioiden ero tulehdusvasteeseen diabeetikoilla (mustat palllot) ja terveillä (valkoistet pallot). Huomaa, ettö asteikot eivät ole yhteismitallisia jokaisen paneelin kohdalla (vasen vs oikea). Lähde: Nappo et al. 2002
Ranskalaisessa tutkimuksessa havaittiin, että IL-6 lisääntyy sekä miehillä että naisilla runsasrasvaisen ruuan jälkeen, mutta TNF-α vähenee lähtötilanteeseen nähden. Lisäksi tässäkin tutkimuksessa havaittiin, että (esi)diabetesta sairastavilla aterianjälkeiset tulehdusvasteet ovat suuremmat. Payette et al. 2009
Uusimmassa italialaisten liikapainoisilla tehdyssä tutkimuksessa runsasrasvainen ateria lisäsi paitsi IL-6 pitoisuutta myös TNF-α 8 tunnin ajan (Miglio et al. 2012). Tässä tutkimuksessa koehenkilöille syötettiin ruoka-annos jossa oli paitsi 80 g rasvaa myös n. 120 g hiilareita ja n. 50 g proteiinia. Kyseessä oli todellisuudessa paitsi runsaasti rasvaa myös runsaasti hiilareita ja proteiinia sisältävä ruoka-annos, vaikka tutkimuksen otsikko lukee vain ”high fat meal”. Tässä tutkimuksessa havaittiin myös erikoinen piirre, runsasrasvainen ateria lisäsi uraatin eli virtsahapon endogeenistä tuotantoa. Uraatti on anti-inflammatorinen aine, ja koholla esim. kihdissä ja munuaisten vajaatoiminnassa. Lisäksi toisenkin endogeenisen antioksidantin tiolin, määrä lisääntyi. Tämä viittaa siihen, että elimistö pyrkii puolustautumaan tulehdusrasitusta vastaan sisäsyntyisin keinoin, siis lisäämällä uraatin ja tiolin erittämistä.
”Rasvarasitus”
Aivan samalla tavalla kuin on olemassa sokerirasitus (OGTT, oral glucose tolerance test kuvassa yllä), on myös rasvarasitus (englanniksi fat challenge). Joidenkin tutkijoiden mielestä suuri rasva-annos kertaistumalta on keholle niin suuri rasite (stressor engl.), että rasvarasitus on hyvä testi minkä tahansa ruokavalion terveellisyysominaisuuksien mittaamiseen. Koehenkilöt altistetaan tiettyjen ruokavaliojaksojen jälkeen rasvarasitukselle ja katsotaan miten erilaiset tulehdus-, oksidatiivisen stressin ja metabolian muuta merkkkiaineet muuttuvat eri ruokavaliojaksojen jälkeen. Mitä enemmän positiivisia muutoksia rasvarasituksen yhteydessä tapahtuu, sen terveellisempänä ruokavaliota voidaan pitää. Joidenkin tutkijoiden mukaan, rasvarasituksen aikana tapahtuvat muutokset saattavat kuvastaa paremmin elimistön tasapainotilaa kuin paastotilanteen mittarit. (Pellis et al. 2011)
Rasvan laatua koskevat väestötutkimukset
Rasvaa koskevia väestötutkimuksia on käyty läpi viime vuonna julkaistussa kirjallisuuskatsauksessa (Calder et al. 2011). Katsauksen mukaan (taulukko 13, s.39). on olemassa 12 väestötutkimusta, joissa rasvan laatua ja tulehdusmarkkereita on tutkittu. Mukana olleet tutkimukset koskettivat pääasiassa yli 50-vuotiaita, joskin yksi lapsia ja kaksi keski-ikäisiä koskettanutta tutkimusta oli mukana. Mukana oli terveillä, lihavilla ja sydänsairauksista kärsivillä tehtyjä tutkimuksia. Keräsin näistä tutkimuksistaneöjön eniten käytetyn tulehdusmarkkerin tiedot (CRP, IL-6 , TNF-α ja V/ICAM-1). Rasvojen saantia kuvasti eri rasvahappojen pitoisuus seerumissa, granylosyyteissä tai ihonalaisessa rasvakudoksessa.
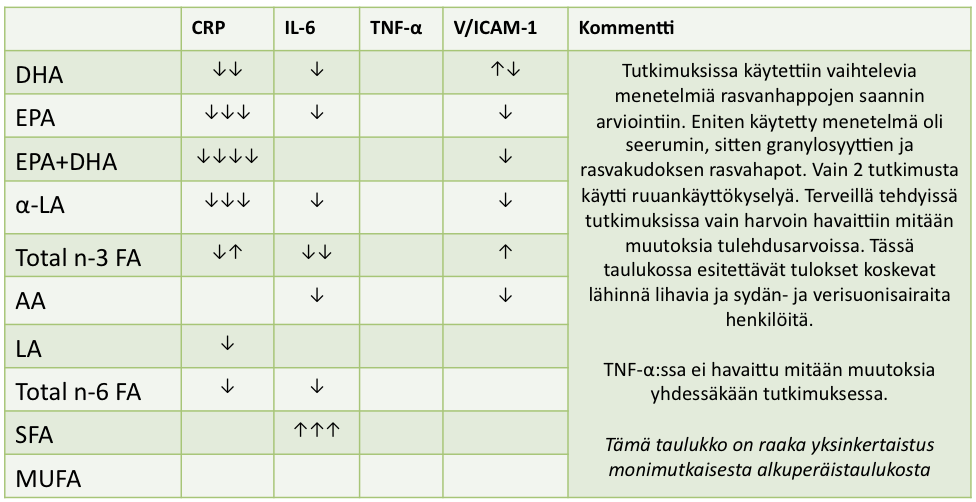
Nuoli kertoo lisääntyikö vai vähenikö jokin tietty tulehdusarvo. Neutraalia eli nollatuloksia ei esitelllä taulukossa. Yksi nuoli tarkoittaa yhden tutkimuksen havaintoa. Perustuu 12 väestötutkimukseen. Lähde: Calder et al. 2011
Edellisessä kuvassa merkillepantavaa on, että väestötutkimuksissa ei tutkittu MUFA:n vaikutuksia. Toinen merkillepantava asia on, että TNF-α:ssa ei tapahtunut muutoksia. Tulehduksen määrä eli magnitudi vaikutti olevan melko vähäinen. Useissa tutkimuksissa ero havaittiin yhdessä merkkiaineessa vaan ei kaikissa
Sivulöydöksenä mielenkiintoinen tutkimus. Aspiriini (ASA) anti-iflammatorinen lääke, jota käytetään runsaasti sydän- ja verisuonitaudista kärsivillä. Osa ihmisistä, ja erityisesti diabeetikot, ovat kuitenkin resistenttejä sille. Toisin sanoen diabeetikoilla aspiriini ei vaikuta normaalistii veren hyytymistä ehkäisevästi. Uudessa tutkimuksessa havaittiin, että erittäin suuri tyydyttyneen rasvan kerta-annos heikensi merkittävästi aspiriinin tehoa veren hyytymisen estossa (Yassine et al. 2011). Jos tämä tulos voidan toistaa pidempikestoisissa tutkimuksissa, tämä tarkoittaa, että suuri määtä tyydyttynyttä rasvaa estää ASA:n tehoa.
Tyydyttynyt rasva lisää tulehdusta, yhden aterian kokeet
Masson & Mensink et al. 2011. Tässä tutkimuksessa hollantilaiset tutkijat syöttivät koehenkilöille (n=13) kertaluonteisesti muffuinsikoeaterian, jossa oli rasvaa 50 grammaa. Rasva oli joko tyydyttynyttä rasvaa (voita) tai monityydyttymätöntä (auringonkukkaöljymargariinia). Koehenkilöt olivat liikapainoisia miehiä, joiden tulehdusarvojen vasteita seurattiin 8 tunnin ajan. Tutkimus kertoo vain yhden koeaterian vaikutuksesta, kun taustaruokavaliota ei muutettu.
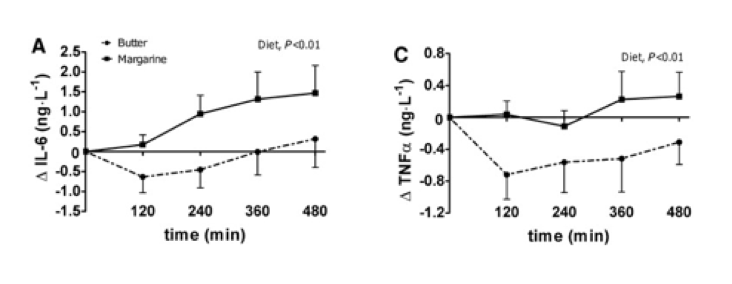
Aurinkokukkaöljymargariinin ja voin vaikutus aterianjälkeisiin tulehdusarvoihin. Lähde: Masson&Mensin 2011
Tutkimuksessa havaittiin, että aterianjälkeinen inflammaatio muuttui selvästi epäedullisempaan suntaan voita sisältäneen muffinsiaterian jälkeen kuin margariinimuffinsin jälkeen. IL-6:n ja TNF-α:n lisäksi myös VCAM-1 oli alempana margariinin jälkeen. Millään tulehdusmittarilla mitattuna voi ei pärjännyt paremmin. Huomioitavaa on, että vaikutus kesti koko mittausjakson ajan eli 8 tuntia aterian nauttimisesta. Glukoosi ja insuliinivasteissa ei ollut eroja. Tutkimus kertoo vain yhden koeaterian vaikutuksesta, kun taustaruokavaliota ei muutettu.
Tulk & Robinson 2009 tekivät tutkimuksen, jossa seurattiin rasvarasituksen (50 g) jälkeisiä tulehdusvasteita metabolisesta oireyhtymästä kärsivillä henkilöillä, kun testiaterioiden n-6 ja n-3 rasvahappojen suhteita muutetaan. Vertailun kohteena oli seuraavat suhteet; n-6/n-3= 20:1 ja 2:1. Varsin monet ovat olleet sitä mieltä, että terveydelle ja erityisesti tulehdusarvoille 2:1 -suhde olisi parempi. Tässä tutkimuksessa yhden koeaterian rasvahappokoostumus ei kuitenkaan vaikuttanut lainkaan tulehdusarvoihin. Tutkimus kertoo vain yhden koeaterian vaikutuksesta, kun taustaruokavaliota ei muutettu.
Peairs et al. 2011 Tässä tutkimuksessa verrattin omega-3 rasvahapoilla, tyydyttyneillä rasvahapoilla ja kertatyydyttymättömillä rasvahapoilla (raffinoitu oliiviöljy) painotetun rasvarasituksen vaikutuksia aterianjälkeiseen inflammaatioon. Kokeeseen osallistui 11 lihavaa henkilöä. Kuusi tuntia aterian jälkeen kestäneessä seurannassa ei havaittu eroaja CRP:ssä eikä TNF-α:ssa. Sen sijaan ICAM-1 lisääntyi tyydyttynyttä rasvaa sisältäneen koeaterian jälkeen.Tutkimus kertoo vain yhden koeaterian vaikutuksesta, kun taustaruokavaliota ei muutettu.
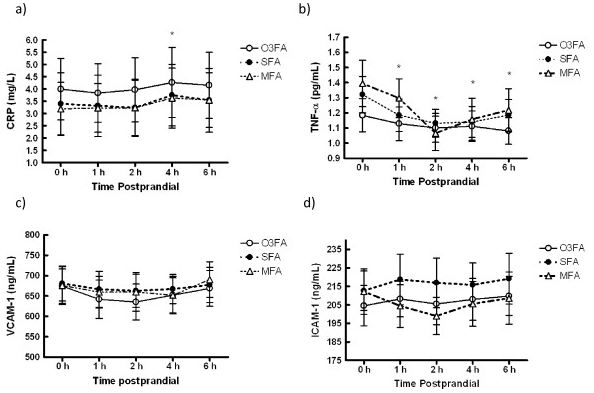
Omega-3, SFA ja MUFA-rasvahappojen vaikutukset tulehdusarvoihin. Vain ICAM-1 koskevat arvot ovat tilastollisesti merkitseviä. Peairs et al. 2011
Manning et al. tutkimuksessa (2008) verrattiin oliiviöljyn, rypsiöljyn sekä voin vaikutuksia aterianjälkeisiin tulehdusarvoihin (IL-6 ja TNF-α) lihavilla naisilla. V- tai I-CAM:ia ei tutkittu. Ryhmien välillä ei havaittu mitään eroja tulehdusarvoissa. Rasva-annos oli 0,6 g rasvaa/painokilo eli tavanomainen n. 50 g/kerta. Tutkimus kertoo vain yhden koeaterian vaikutuksesta, kun taustaruokavaliota ei muutettu.
Papageorgiou et al. (2011). Tässä tutkimuksessa kreikkalaisille koehenkilöille syötettiin 50 ml erilaisia öljyä, jonka jälkeen seurattiin tulehdusvasteita 3 tunnin ajan. VCAM-1 ei muuttunut minkään öljyn vaikutuksesta. Sen sijaan ICAM-1 väheni kaikkien öljyjen vaikutuksesta. TNF-α väheni extra neitsyt oliviöljyn, turskaöljyn ja soijaöljyn, vaan ei maissiöljyn vaikutuksesta. Vahinko ettei näiden neljän öljyjen lisäksi ollut mukana voita.
Päivitys 5/2013: Espanjanlaisessa aterikokeessa extra neitsytoliiviöljy vähensi aterianjälkeisiä tulehdusarvoja verrattuna raffinoituun oliiviöljyyn (Pacheco et al. 2007). Ennen ateriaa oli yhden viikon ”sydänystävällinen ruokavalio”.
Omega-6 rasvahapot neutraaleita, viikkojen mittaiset RCT-tutkimukset
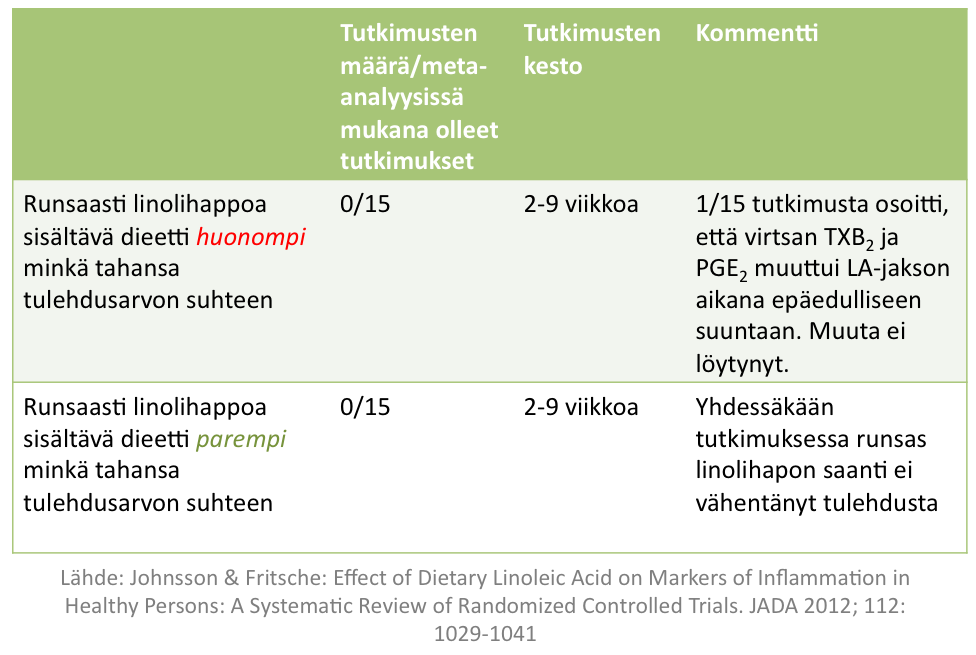
Juuri ilmestyneessä meta-analyysissä käsiteltiin satunnaistettujen tutkimuksien tulokset tilanteessa, jossa ruokavaliota rikastettiin linolihapolla (Johnson & Fritsche 2012).
Kaikki 15 meta-analyysissä ollut tutkimusta osoittivat, että linolihapolla ruokavalion rikastaminen ei vaikuta tulehdusarvoihin muutamia viikkoja kestäneissä tutkimuksissa. Tulos oli CRP:n, TNF-α:n ja IL-6:n sekä PAI:n osalta täysin selvä -ei mitään eroa. Virtsasta löytyi vähemmän TXB2:ta ja enemmän PGE2:ta kahdessa tutkimuksessa linolihappojakson aikana. Käytetyt linolihappoannokset olivat keskimäärin 20-30 grammaa /pv linolihappojakson aikana (enimillään 50 g/pv) ja kontrolliruokavalioissa 0-5 g (enimillään 10 g/pv). Suomalaisten linolihapon saanti on nykyisin n. 10 grammaa per päivä.
Meta-analyysi kertoo siis tilanteesta, jossa suomalaiset lisäisivät linolihapon saantia 2-3 kertaiseksi nykyisestä. Tällaisella lisäyksellä ei siis olisi vaikutusta verestä mitattaviin tulehdusarvoihin ainakaan muutaman viikon aikana.
Tutkimukset jotka eivät olleet mukana edellä mainitussa meta-analyysissä
Bjermo et al. (2012) tutkimuksessa verrattiin liikapainoisilla koehenkilöillä voipainotteisen ja aurinkokukkaöljyyn painottuvan ruokavalion vaikutuksia veren tulehdusmarkkereihin (ja mm. maksan rasvoittumiseen). Tutkimus ei kerennyt mukaan edellä mainittuun meta-analyysiin. 10 viikon seurannassa auringonkukkaöljyhoito kohensi joitakin tulehdusarvoja (IL-1RA ja TNF-R2) vaan ei CRP-arvoa. Tämä on yksi harvoista pidempikestoisista tutkimuksista (vs edellä olleet yhden aterian tutkimukset) ja sen tutkimukset ovat linjassa edellä esitettyjen tutkimuksien kanssa. Runsaasti tyydyttynyttä rasvaa sisältävä ruokavalio voi aiheuttaa lievän tulehdusvasteen, kun taas linolihappopitoinen tyydyttymätön rasva saattaa olla neutraalia tai lievästi anti-inflammatorista.
Gillingham et al. (2011) tutkimuksessa korkeasta kolesterolista kärisville koehenkilöille syötettiin joko ALA-pitoista pellavansiemenöljyä, rypsiöljyä tai näiden yhdistelmää kuuden kuukauden ajan. Tulehdusmarkkereissa ei yleisesti ottaen tapahtunut muutoksia (pl. E-selektiini, joka väheni pellavansiemenjaksolla). Rypsiöljy ei siis sellaisenaan vaikuttanut terveiden korkeasta kolesterolista kärsivien tulehdukseen. Tässä rypsiöljyssä oli vielä enemmän öljyhappoa kuin suomalaisessa rypsiöljyssä.
Petersson et al. (2010) LIPGENE -tutkimuksessa syötettiin vaihteleva määrä MUFA:aa, SFA:ta ja omega-3 rasvahappoja (EPA/DHA) metabolisesta oireyhtymästä kärsiville 3 kuukauden tutkimuksesssa. Tutkimuksen lopussa tulehdusmittareissa ei ollut eroa paastotilanteessa. Tämän tutkimuksen mukaan tyydyttyneet rasva eivät siis aiheuta tulehdusvastetta, eikä omega-3 rasvahapot sitä vähennä.
Edellä mainitusta LIPGENE-tutkimuksesta on tehty myös aterianjälkeisiä vasteita koskevat tulokset. Niissä huomattiin, että tyydyttynyttä rasvaa runsaasti sisältävä ruokavalio lisäsi aterianjälkeistä tulehdusta. Myös erittäin vähärasvainen ruokavalio lisäsi tulehdusvasteitä, eikä omega-3 rasvahappojen lisääminen estänyt aterianjälkeisiä tulehdusvasteita. Sen sijaan kasviöljyjä (ilmeisesti oliiviöljy) sisältävien ruokavalioiden aikana aterianjälkeiset inflammaatiovasteet vähenivät. Tutkimus kesti 12 viikkoa. (Cruz-Teno et al. 2012)
Fitó et al. (2008). Tässä tutkimuksessa verrattiin raffinoitua oliiviöljyä ja extra virgin oliiviöljyä, jossa on paljon polyfenoleita sydänsairailla miehillä kolmen viikon ajan. Raffinoitu oliiviöljy ei vaikuttanut tulehdusmarkkereihin, mutta extra virgin oliiviljy vähensi IL-6:n ja CRP:n määrää. Tämä käsittääkseni ainoa työ, jossa on verrattu puhdistettua oliiviöljyä ja ekstra neitsytoliiviöljyä tulehdusmarkkereiden suhteen.
Arakidonihappo (AA)
Yllättävää kyllä arakidonihapollakin on tehty jokunen tutkimus. Pohjatiedoksi se, että arakidonihapon saanti on hyvin vähäistä useimpiin muihin rasvahappohin verrattuna. Normaali arakidonihapon saanti lienee n. 0,2 g/pv. Vuonna 2007 Roberts et al. todistivat, että arakidonihappo annoksella 1 g/pv lisäsi paitsi kehorakentajien voimantuottoa vähensi myös IL-6:ta. Haittavaikutuksia ei ilmennyt.
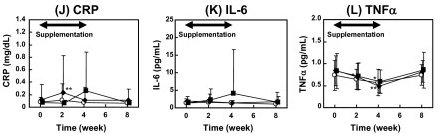
Japanilaiset tutkijat puolestaan syöttivät AA:ta annoksella 0,27 tai 0,72 g/pv vanhuksille kahdeksan viikon ajan. Tutkijoiden mukaan arakidonihappo ei lisännyt tulehdusta kehossa. (Kakutani et al. 2011, kuva alla)
Näiden kahden tutkimuksen valossa arakidonihappo edes sellaisenaan ei todellakaan ole mitään myrkkyä. Tutkijat itse päättelevät:
”In summary, blood parameters of cardiovascular, inflammatory and allergic diseases, as well as urinary and plasma ARA metabolites did not change in Japanese healthy elderly participants who consumed ARA-enriched oil (240 or 720 mg/day of ARA) for 4 weeks although plasma ARA levels significantly increased.”
Arakidonihapon lähteitä ravinnossa ovat kana, punainen liha ja kananmuna.
Omega-3 rasvahapot, viikkojen tutkimukset
Tästä asiasta on ilmestynyt juuri uusi systemoitu kirjallisuuskatsaus (Rangel-Huerta et al. 2012). Tässä katsauksessa oli mukana kaikkiaan 26 eri tutkimusta, joiden kesto vaihteli tyypillisesti 2-12 viikon välillä. Mukana oli terveillä, sydänsairailla sekä muissa sairauksissa tehtyjä tutkimuksia. Tämän katsauksen mukaan:
- Omega-3 rasvahapot eivät muuta terveillä ihmisillä tulehdusmarkkereita (ehkä siksi että terveillä tulehduksen merkkiaineeet ovat luonnostaan hyvin alhaisella tasolla). Yhdessäkään kuudesta tutkimuksesta muutosta ei havaittu.
- Rasittavan liikunnan jälkeiseen tulehdukseen saatiin ristiritaiset tulokset. Toisessa tutkimuksessa EPA/DHA 4 g/pv vähensi tulehdusta liikunnan jälkeen ja toisessa ei havaittu muutosta
- Sydänsairailla omega-3 supplementaatio vähensi useassa, vaan ei kaikissa, tutkimuksissa CRP:tä ja TNF-α:aa. Sen sijaan sICAM ei muuttunut kuin yhdessä tutkimuksessa. Tulos näytti paremmalta vähintään 12 viikkoa kestäneissä tutkimuksissa
- Munuaistaudissa ja Alzheimerintaudissa (yhteensä kolme tutkimusta) omega-3 rasvahapot vähensivät tuelhduksen merkkiaineita
- Kriittisesti sairailla (pankreatiitti) omega-3 rasvahapot vähensivät tulehdusmarkkeita
Tässä katsauksessa loppupäätelmänä oli, että omega-3 rasvahapot saattavat vähentää tulehdusta eri sairaustiloissa, mutta tieteellinen näyttö ei ole vakuuttavaa. Terveillä ei havaittu muutoksia tulehdusarvoissa.
Omega-3 rasvahapoilla tehdyt pitkät tutkimukset
On harmillista, että moderneissa ja pitkäkestoisissa kalaöljyä ja α-linoleenihappoa koskevissa kovien päätetapahtumien tutkimuksissa ei ole mitattu tulehdusmarkkereita, edes CRP:tä. Nämä tutkimukset olisivat olleet otollinen tapa varmistu, onko omega-3 rasvahapoilla riittävän kauan pillerinä annettuna hyötyä tulehdusarvoihin.
Näiden tutkimuksien keskeiset sairastuvuustulokset on esitetty hiljattain ilmestyneessä 14 tutkimuksen koosteessa eli meta-analyysissä (Kwak et al. 2012). Sen mukaan omega-3 rasvahappojen käyttö ei vähennä sydäntapahtumia sydänsairailla. Koosteesta puuttui JELIS- ja GISSI -tutkimukset, koska ne eivät olleet sokkoutettuja eivätkä ne olleet lumekontrolloituja. Juuri näissä kahdessa tutkimuksissa kalaöljy näytti puolestaan vähentävän sydäntapahtumia.
Kertatyydyttymätön rasva, MUFA
Kertatyydyttymättöntä rasvaa (MUFA) on pidetty tulehduksen kannalta neutraalina. Toisaalta extra virgin oliiviöljy sisältää runsaasti polyfeneoleita, joilla on anti-inflammatorisia vaikutuksia.
Löysin ainoastaan kolme tutkimusta, jossa on käytetty raffinoitua oliiviöljyä. Niissä yhdessäkään raffinoitu oliiviöljy ei vaikuttanut tulehdusvasteisiin. Tholstrup et al.(2011) todisti, että erittäin suuri annos, 1 g/kg oliiviöljyä, kerta-annoksena ei lisää lainkaan terveiden naisten CRP:tä tai IL-6:ta. Tämä on täysin vastakohtainen tulos mitä tyydyttyneellä rasvalla vastaavalla annoksella (kermalla) on saatu, kuten edellä on esitelty. Edellä referoidussa ruotsalaisessa tutkimuksessa havaittiin, että MUFA:lla rikastettu ruokavalio ei vaikuttanut kolmen kauden kohdalla tulehdusarvoihin Petersson et al. (2010) . Myös kreikkalainen tutkimus raffinoidulla oliiviöljyllä puoltaa MUFA:n neutraaliutta, ja toisaalta neitsytoliiviöljystä löytyvien polyfenolien edullista vaikutusta tulehdukseen Fitó et al. (2008).
Juuri ilmestyneessä satunnaistetussa amerikkalaisessa tutkimuksessa havaittiin, että extra virgin oliiviöljy puoli vuotta käytettynä vähentää tulehdusta ateroskleroosista kärsivillä potilailla (Widmer et al. 2012).
Kertatyydyttymätöntä rasva sinänsä vaikuttaa näiden tutkimuksien perusteella neutraalilta, mutta extra virgin oliiviöljystä saatavat polyfenolit vähentävät tulehdusta. Polyfenoleista erikseen lisää myöhemmässä kirjoituksessa.
Trans-rasva ja CLA
Transrasvahapot ovat tämänpäivän käsityksen mukaan ihmisille kaikista ruokavalion rasvahapoista haitallisimpia, koska ne paitsi lisäävät LDL-kolesterolia alentavat myös HDL-kolesterolia (toisin kuin esim. tyydyttynyt rasva). Transrasvahappojen on sanottu myös lisäävän tulehdusta (Mozaffarian et al. 2006). Transrasvan saanti on Suomessa vähäistä.
Konjugoitu linolihappo (CLA) on luonnostaan maidossa esiintyvä trans-rasvahappo. Siitä on tehty myös kaupallisesti myynnissä oleva ravintolisä, jota on markkinoitu laihduttajille ja urheilijoille. Tämä ravintolisänä myytävä tuote on yksi isomeeri samasta maidon CLA:sta. Ravintolisänä käytettävällä CLA:lla ei ole havaittu juurikaan vaikutusta tulehdusarvoihin terveillä ihmisillä (Ramakers et al. 2005, Tricon et al. 2006, Asp et al. 2011, Smit et al. 2011), joskin yhdessä tutkimuksessa tulehdusarvot lisääntyivät (Steck et al. 2007). Sen sijaan metabolisesta oireyhtymästä kärsivillä CLA lisää tulehdusta joidenkin tutkimuksien mukaan (Riserus et al. 2002, Riserus et al. 2004), kun taas aikuistyypin diabeetikoilla se ei lisää tulehdusta (Moloney et al. 2004). Ristiriitaiset tulokset voivat selittyä erilaisella käytetyllä isomeerilla tai niiden kombinaatiolla (c9,t11 vs t10,c12).
Kolesteroli
Kolesteroli ei ole varsinaisesti ravinnon rasva. Korkea LDL ”paha kolesteroli” liitetään tyydyttyneen rasvan määrään ruokavaliossa. Siten kolesterolin pintapuolinen käsittely on tarpeen. Tutkija Pauli Ohukainen esitti Varpu Tavin blogissa lähinnä koe-eläin töihin perusten, että veren korkea kolesterolipitoisuus ruokkii inflammaatioprosessia. Koe-eläinten ravintoa muuttamalla on voitu kääntää kohonnut veren kolesterolipitoisuus laskuun ja samalla vähentää jo syntyneitä ateroskleroottisia muutoksia sekä tulehdusta.
Mielestäni ongelma näissä tutkimuksissa on se, että edes koe-eläinten ravinnolla ei voi laskea veren kolesterolia ilman muutosta ravinnon rasvojen laadussa, hiilihydraateissa, kuidussa ja/tai energianmäärässä. Siten ei voitane väittää, että ravintomuutosten avulla saatava muutos veren kolesterolissa olisi yksistään tai edes keskeisin vaikuttaja inflammaatiossa. Mukana on muita samanaikaisia tässä kirjoituksessa kuvattuja mekanismeja, esim. LPS:n imeytymisen lisääntyminen ja desaturaasientsyymien toiminnan muuttuminen.
Keskeistä ja tärkeintä kuitenkin on, että korkea veren kolesterolipitoisuus lisää myös muuntuneiden LDL-partikkelein (hapettuneiden ja glykoituneiden) määrää. Muuntunut LDL ruokkii puolestaan erilaisia tulehdusmuutoksia verisuonen seinämässä (Leonarduzzi et al. 2012). Voitaneen siten väittää, että kaikki ravintotekijät, jotka johtavat hapettuneen tai glykoituneen LDL-kolesterolin syntyyn johtavat myös verisuonessa majailevan tulehduksen lisääntymiseen.
Tulehdukselliset suolistosairaudet
Vuonna 2010 ilmestyneessä Hou et al. väestötutkimuksien meta-analyysissä havaittiin, että runsas linolihapon saanti ruokavaliosta sekä suuri rasvan osuus ruokavaliossa sinänsä näyttää lisäävän tulehduksellisten suolistosairauksien (IBD) riskiä (=Crohnin tauti ja haavainen paksusuolen tulehdus). Sen sijaan omega-3 rasvahappojen saannilla ei näyttänyt olevan yhteyttä sairauksien ilmaantumiseen. Myöskään tyydyttynyt rasva ei liittynyt IBD:n riskiin.
Tulehduksellisissa suolistosairauksissa on kokeiltu omega-3 rasvahappoja, vaan ei ilmeisestikään linolihappoa tai tyydyttyneellä rasvalla rikastusta. Omega-3 rasvahapoilla tehdyt tutkimukset ovat olleet osin pettymyksiä, osin onnistumisia. Kliinisesti merkittäviä tuloksia (oireiden paranemista) ei saavutettu viidessä hyvin tehdyssä kliinisessä tutkimuksessa annoksilla 3-5 g/pv. (Feagan et al. 2008, Lorentz-Meyer 1996, Loschke et al. 1996, Greenfield et al. 1993, Howthorne et al. 1992).
Toistaalta yksi NEJM:ssä julkaistu tutkimus osoitti, että kalaöljystä annoksella 3 grammaa päivässä (tyypillisesti kuusi kapselia/pv) on hyötyä Crohnin taudin oireiden vähentämisessä (Beluzzi et al. 1996). Lisäksi yhdessä lapsilla tehdyssä tutkimuksessa 3 gramman päivittäinen paransi Crohnin tautipotilaiden oirekuvaa (Romano et al. 2005).
Lisäksi eräs tutkimus osoitti haavaisesta paksusuolen tulehduksesta kärsivien hyötyvän omega-3 rasvahapoista 4 g/pv annoksella (Asian et al. 1992). Neljä kuukautta kestäneessä satunnaistetussa kokeessa kalaöljy annoksella 4 g/pv vähensi suolistovaurioita haavaisessa paksusuolen tulehduksessa histologisin näyttein varmennettuna (Stenson et al. 1992)
Siten kalaöljystä voidaan päätellä, että se luultavasti joko neutraali tai lievästi hyödyllinen Crohnin taudissa ja mahdollisesti hyödyllinen haavaisessa paksusuolen tulehduksessa, kun annos on vähintään 3 grammaa päivässä. Valitettavasti näissä(kään) tutkimuksissa ei mitattu CRP:tä, IL-6, TNF-α:aa tai muita tulehdusmittareita. Muista rasvoista ei ole enempää kerrottavaa tässä suhteessa.
Nivelreuma
Vuonna 2007 ilmestyneen meta-analyysin mukaan omega-3 rasvahapposupplementaatio vähentää reumaan liittyvää nivelkipua ja tulehduskipulääkkeen tarvetta (Goldberg ja Katz). Tänä vuonna ilmestyneen meta-analyysin mukaan on olemassa melko yhdenmukainen näyttö siitä, että reumapotilaat hyötyvät omega-3 rasvahapposupplementaatiosta, joskin oireiden vähentyminen on parhaimillaankin vain kohtalaista (Miles & Calder 2012). Muiden rasvahappojen vaikutuksesta reumaan ei juuri tiedetä.
Syöpä
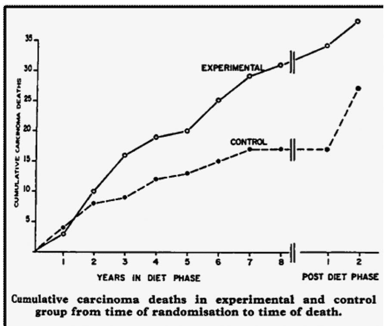
Omega-6 rasvahappojen on väitetty lisäävän joidenkin syöpien riskiä. Erityisen puuhakas tällä rintamalla on suosittu amerikkalainen bloggaaja ja perustutkija (lue koe-eläintutkija) Chris Masterjohn. Myös tunnettu Välimeren ruokavalion tutkija Michel de Lorgeril on huolissaan omega-6 rasvahappojen syöpävaikutuksista.
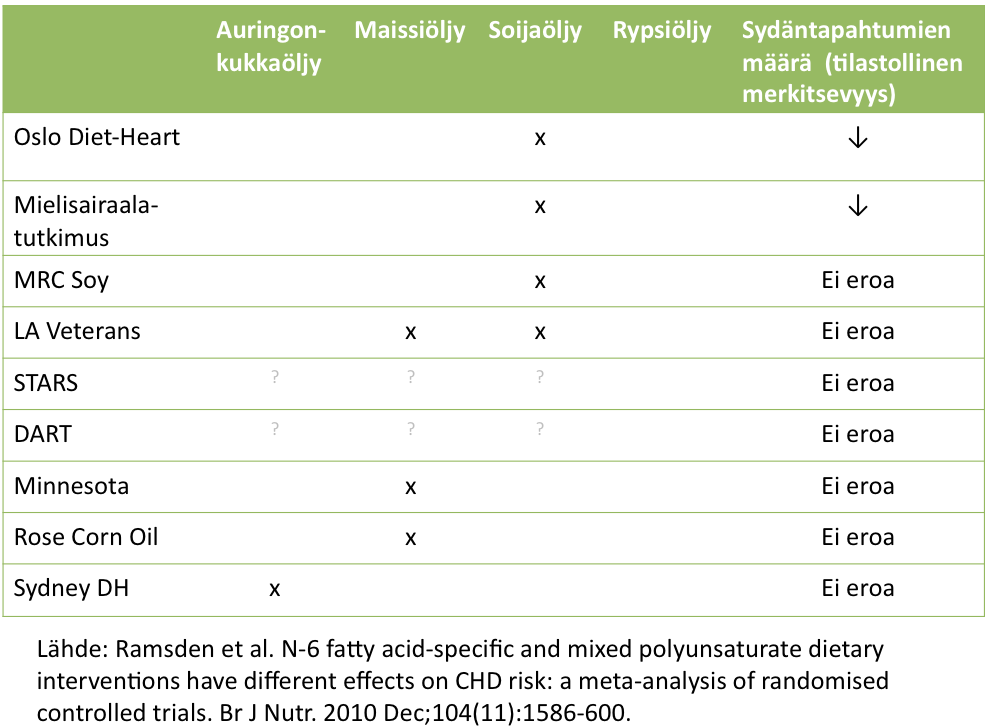
Masterjohnin mukaan pitkäaikainen runsas omega-6 rasvahappojen saanti lisää syövän riskiä. Masterjohnin esittää väitteensä tueksi pääasiassa koe-eläintöitä ja yhden kliinisen päätetapahtumatutkimuksen LA Veterans, jossa tutkimuksen loppuvaiheessa lisääntyi syövän esiintyvyys soija- ja maissiöljyä käyttävillä (ei tilastollisesti merkitsevästi). De Lorgeril esittää, että Lyon Heart -tutkimuksessa ja LA Veterans -tutkimuksessa olisi tullut esille viitteitä (ei tilastollisesti merkitseviä) syövän lisääntymisestä.
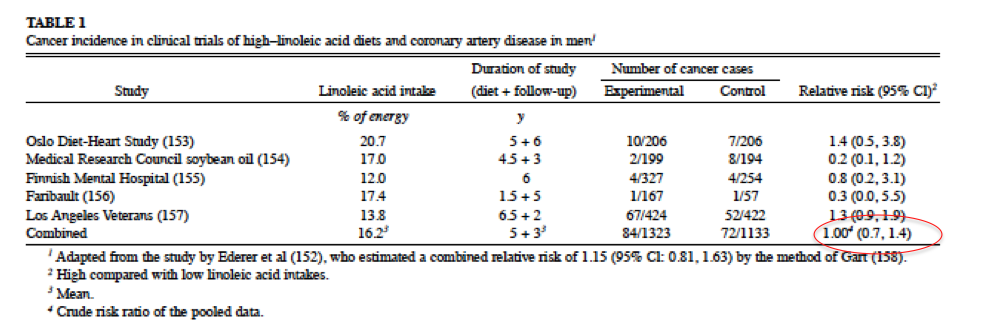
Ongelma on, että Masterjohn ja de Lorgeril sulkee silmänsä vastakkaiselta evidenssiltä. Hollantilaiset tutkijat tekivät jo vuonna 1993 meta-analyysiin suurista klassisista rasvatutkimuksista joista yksi siis on juuri tuo LA Veterans (Zock & Katan 1993). Samassa yhteydessä pengottiin myös prospektiiviset kohorttitutkimukset. Johtopäätös: omega-6 rasvahapot tai ainakaan niistä yleisin linolihappo ei lisää syövän vaaraa.
Tämän lisäksi toinen hollantilaisten tutkijoiden ryhmä selvitti onko ihmisen rasvakudoksesta löytyvä omega-6 rasvahappojen määrä yhteydessä syöpään (Bakker et al. 1997). Suomalaisilla ensinnäkin oli vain puolet israelilaisten omega-6 rasvahappomäärästä rasvasoluissa. Toiseksi, omega-6 rasvahapoilla ja syövällä ei ollut yhteyttä.
Olen kuitenkin Masterjohnin ja de Lorgerilin kanssa yhtä mieltä, että syöpä tarvitsee erittäin pitkän ajan kehittyäkseen (usein yli 10 v), ja tähän saakka tehdyt ravitsemustutkimkset voivat olla liian aivan liian lyhyitä varmentaakseen esim. eri rasvojen vaikutukset syövän ilmaantumiseen. Kokonaan toinen seikka on se, tuleeko koskaan riittävän pitkää syöpätutkimusta kustannus- ja komplianssisyistä johtuen.
Sydänsairaudet
Kaikki edellä olevat tutkimukset ovat olleet lyhytkestoisia tai perustuneet väestötutkimuksien havoinnoivaan dataan. Tällaisiin liika usko ei ole viisasta. On esimerkiksi epäselvää, mikä merkitys on sillä, että yksi tulehdusarvo värähtää hiukan ylöspäin samalla kun useimmissa muissa ei tapahdu yhtikäs mitään muutosta. Kaikkinensa muutokset ovat erittäin pieniä esim. verrattaessa radikaaliin laihtumiseen (CRP tippuu jopa 80 %, Ahmadi et al. 2011).
Rasvat ovat oikeastaan ainoa kapitteli ravitsemuksessa, jota on tutkittu useissa satunnaistetuissa tutkimuksissa sydänkuolemat ja -infarktit päätetapahtumina. Tällaiset tutkimukset ovat niitä kovimman näytön tutkimuksia. Nämä varhaiset ja edelleen tärkeät tutkimukset ovat osoittaneet jo n. 40 vuotta sitten, että rasvojen saanti erittäin jyrkästi muuttamalla on vaikea saada aikaan johdonmukaista yhdensuuntaista muutosta sydänterveydessä (kuva alla). Olen kirjoittanut näistä tutkimuksista mm. tämän yhteenvedon.
Tutkimusten tulos on seuraavaa: runsas omega-6 rasvahappoja sisältävän kasviöljyn painotus saattaa vähentää hiukan sydäntapahtumia (14 %), jos sen käyttöä lisätään maitotuotteiden ja lihan rasvan kustannuksella. Toisinpäin näyttöä on aivan anekdotaalista, eli kasviöljyt erittäin suurilla annoksilla eivät näytä lisäävän sydän- ja verisuonitautitapahtumia. (Ramsden et al. 2010).
Yhteenvetona: a) kovimman näytön pitkäkestoiset satunnaistetut sydänsairaustutkimukset ja b) lyhytkestoiset satunnaistetut tutkimukset sekä c) väestötutkimukset eivät tuota selvää näyttöä siitä, että omega-6 rasvahapoillla olisi selvää inflammatorista vaikutusta, joka heijastuisi selvästi esim. sydänterveydessä.
”New tvist in an old tale”
Moni saattaa kaivata selitystä sille, miksi omega-6 rasvahapot eivät olekaan niin selkeästi tulehdusta aiheuttavia. Sille on käsittääkseni kolme päällimmäistä selitystä:
A) Linolihapon määrän lisääminen ravinnossa ei lisääkkään arakidonihapon määrää veressä, kuten on kuviteltu (ja biokemian oppikirjat kertovat)
B) Arakidonihapolla on tiettyjä anti-inflammatorisia vaikutuksia, jotka ovat jääneet vähälle huomiolle. Edes arakidonihapon syöttäminen kolme kertaa tavanomaista suuremmilla annoksilla ei johda inflammaatioon
C) Myös omega-3 rasvahapoilla voi olla lieviä pro-inflammatorisia vaikutuksia, erityisesti EPA:lla
A) Linolihappo ei juurikaan sanele arakidonihappopitoisuuksia elimistössä
Onhan se kummallista, että toisin kuin biokemian kirjat ovat väittäneet, linolihapon saanti ei ole yhteydessä arakidonihapon määrään veressä, eikä siten tulehdukseen. Kliinisiä tutkimuksia siitä, että linolihappo ei lisää arakidonihapon määrää elimistössä on valtavasti. Johnson & Fritsche (2012) toteavat:
”There is now consistent evidence that dietary LA does not unconditionally increase circulating AA concentrations.”
Edellä mainittu lause perustuu mm. uudehkoon 36 kliinistä tutkimusta kattaneeseen systemoituun kirjallisuuskatsaukseen (Rett et al. 2011) Tämän kirjallisuuskatsauksen mukaan on selvästi osoitettu, että länsimaisen ruokavalion yhteydessä linolihapon merkittävä vähentäminen (jopa 10 %:iin vs normaalitilanne) ei vähennä arakidonihapon määrää elimistössä, eikä linolihapon lisääminen (jopa 6-kertaiseksi tavanomaiseen verrattuna) lisää arakidonihapon määrää elimistössä. (Klikkaa kuvaa, open access artikkeli).
Ilokseni huomasin, että samassa katsauksessa annetaan myös pitkään kaipaamani arvio sille miten paljon linolihaposta muuttuu arakidonihapoksi (vetailun vuoksi ALA:sta 5-10 % muuttuu EPA:ksi)
” Intracer studies involving stable isotopes, the estimated fractional conversion of LA to AA was between 0,3 % and 0,6 % [31].”
Arakidonihapon määrää elimistössä säätelee arakidonihapon määrä ruokavaliossa. Arakidonihappoa saamme eläin kunnantuotteista (lähteitä siis liha, makkara, kananmuna, sisäelimet, kana jne.).
B) Arakidonihapon anti-inflammatoriset vaikutukset
Arakidonihappo tuottaa siis 2-sarjan tulehdusta edistäviä prostaglandiineja. Nykyään kuitenkin tiedetään että PGE₂:llä on myös tulehdusta vastustavia ominaisuuksia ja että arakidonihaposta syntyvä lipoksiini A₄ on tulehdusta lievittävä.
”However this is an over-simplification since some actions of eicosanoids are anti-inflammatory (e.g. PGE2 inhibits production of some inflammatory cytokines) and it has been discovered quite recently that PGE2 inhibits production of inflammatory leukotrienes and induces production of inflammationresolving lipoxin A4.”
Näin toteaa Philip Calder (2009) katsauksessaan ”Polyunsaturated fatty acids and inflammatory processes: New twists in an old tale”.
Tässä samaisessa katsauksessa on mielenkiintoinen kohta, jossa todetaan omega-3 rasvahappojen kilpailevan arakidonihapon kanssa paikasta tulehdusolujen fosfolipideissä. Tästä tuloksena on, että arakidonihaposta muodostuu vähemmän tulehdusta aiheuttavia eikosanoideja, jos omega-3 rasvahappoja on riittävästi tarjolla elimistössä (kuva alla).
”The n-3 fatty acids EPA and DHA, are incorporated into inflammatory cell phospholipids in a time- and dose-dependent manner. They are incorporated partly at the expense of AA, but also of other n-6 fatty acids. EPA and DHA inhibit AA metabolism . Thus production of AA-derived eicosanoids is decreased by these n-3 fatty acids; this occurs in a dose-dependent manner. (Lihavointi allekirjoittaneen)
C) EPA:n tulehdusta edistävät vaikutukset
Kuten alla oleva kuva kertoo EPA:sta syntyy lievästi proinflammatorisia prostaglandiineja (3-series PGs) ja leukotrieenejä (5-series LTs). Tämä saattaa selittää sen, miksi kalaöljyn inflammaatiota vähentävät tulokset eivät ole vahvempia ja kliinisissä tutkimuksissa, ehkä reumaa lukuunottamatta, harvemmin yksiselitteisesti hyötyä tuovia. Mielenkiintoista on, kuten edellä tuli juuri esille, EPA:n kohdalla myös se, että se estää arakidonihapon muuttumista voimakkaasti tulehdusta aiheuttaviksi 2-sarjan prostaglandiineiksi ja 4-sarjan leukotrieeneiksi.
Tyydyttynyt rasva
Jos tyydyttynyt rasva suurilla annoksilla aiheuttaa tulehdusta, mikä sitten on ilmiön taustalla? Mekanismeja saattavat olla:
- Suuri tyydyttyneen rasvan kerta-annos lisää LPS:n imeytymistä suolistosta, joka johtaa tulehdukseen laajalti elimistössä Toll-like reseptori 4 -välitteisesti (TLR4). LPS on tulehdusta lisäävää endotoksiini, joka erittyy suoliston bakteereista
- Tyydyttynyt rasva saattaa voimistaa verenkierrossa LPS:n vaikutuksia metaboloitumalla keramideiksi (Chait & Kim 2010)
- Tyydyttynyt rasva estää ALA:n muuttumista EPA:ksi (Das U. 2010 ja Warensjö et al. 2011. )
”… saturated and trans-fats that are known to inhibit the activity of Δ6 and Δ5 desaturases [6,7,16-18] which, in turn, further aggravate their tendency to develop insulin resistance and the metabolic syndrome [67].” (Das 2010)
- Tyydyttynyt rasva saattaa heikentää HDL:n anti-inflammatorisia vaikutuksia (Nicholls et al. 2006)
Tyydyttyneen rasvan vaikutus Δ6 and Δ5 desaturaaseihin oli minulle uutta. Seuraava kuva Das et al. artikkelista kuvaa tilannetta.
Dasin lisäksi tyydyttyneen rasvan negatiivisen vaikutuksen Δ5 desaturaasiin on todennut ruotsalainen Warensjö et al. (2011) kliinisessä tutkimuksessaan. ”Kova rasva” estää siis α-linoleenihapon muuttumista EPA:ksi. Se myös lisää Warensjön mukaan linolihapon muuttumista γ-linoleenihapoksi ja sitä kautta edelleen arakidonihapoksi. Tämä havinto on ristiriidassa alla olevan Dasin koe-eläin ja in vitro -tutkimuksiin perustuvan kuvan kanssa. Dasin mukaan tyydyttynyt rasva vähentää Δ6 desaturaasin aktiivisuutta ja estää siten linolihapon edelleen metaboloitumista. Uskon enemmän kliiniseen ihmisillä tehtyyn tutkimukseen tässä(kin) asiassa.
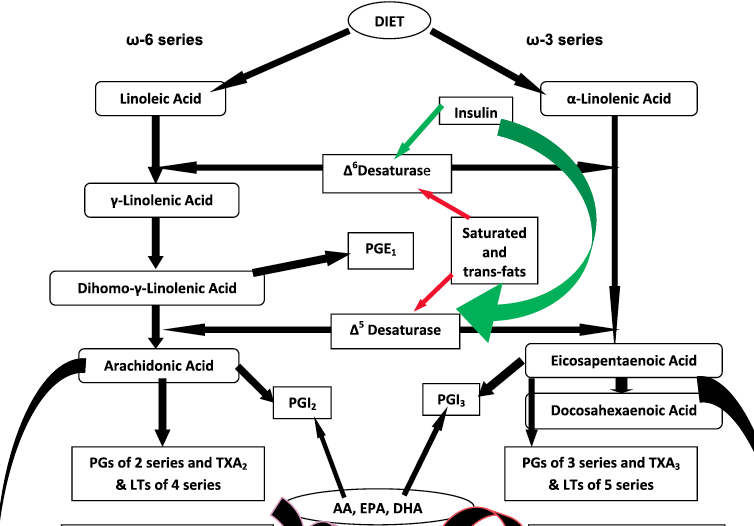
Tyydyttynyt rasva ja trans-rasva heikentää desaturaasientsyymien toimintaa ja vähentää siten ALA:n muttumista EPA:ksi (punaiset nuolet). Lähde: Das U. Lipids Health Dis. 2010; 9: 130.
Lopuksi
Kaikkinensa tämän kirjoituksen keskeinen sanoma on seuraava: Pelkällä rasvan laadulla ei ole niin keskeistä roolia tulehduksen kannalta, kuin usein esitetään. Ruokavalion rasvoja modifioimalla saadut tulehdusmuutokset ovat vähäisiä verrattuna esimerkiksi siihen, miten laihdutuksella voidaan saavuttaa. Tilastollinen merkitsevyys saatetaan saavuttaa, mutta kliininen relevanssi, vaikutuksen käytönnön merkitys on yleensä ollut heiveröinen.
Omega-6 rasvahappojen esittäminen kaikkin turmiollisempana tulehduksen aiheuttajana ja omega-3 rasvahappojen ylistäminen tulehduksen lopullisena ja ainoana helpottajana on väärä.
Näyttää pikemminkin siltä, että tyydyttynyt rasva, ainakin tavanomaista suuremmilla annoksilla, on tulehdusta lisäävä. Aterian jälkeiset rasvarasitukset tehdään tyydyttyneellä rasvalla. Runsaasti tyydyttynyttä rasvaa sisältävä ruoka lisää, ainakin akuutisti, lisää LPS:n imeytymistä, joka lienee yksi keskeinen mekanismi tämän tulehdusvaikutuksen taustalla. LPS puolestaan lisää tulehdusta rasvakudoksessa, maksassa ja verisuonissa. Toinen keskeinen mekanismi saattaa olla se, että tyydyttynyt rasva estää ALA:n muuntumista EPA:ksi ja lisää samalla linolihapon muuttumista arakidonihapoksi. Lopuksi, tyydyttynyt rasva saattaa heikentää HDL-kolesterolin anti-inflammatorisia vaikutuksia.
Tyydyttyneen rasvan vaikutukset tulehdukseen ovat diabeetikoilla selvästi pahemmat kuin terveillä.
Kalan, rypsi- ja pellavansiemenöljyn omega-3 rasvahapot ovat ainakin osittain anti-inflammatorisia. Omega-3 rasvahappojen puuteellinen saanti vaikuttaa erityisen turmiolliselta, koska se johtaa tulehdukseen myös arakidonihapon reitin kautta (klassisen EPA/DHA-reitin lisäksi). Toisaalta, ylenpalttinen omega-3 rasvahappojen saannin lisääminen ei välttämättä tuo selvää lisäetua tulehduksen suhteen, ainakaan terveille.
Kertatyydyttymätön rasva vaikuttaa tulehduksen suhteen neutraalilta. Extra virgin oliiviöljystä saatavat polyfenolit ovat syynä sille, että tämä oliiviöljylaatu vähentää tulehdusta, kun taas puhdistettu eli raffinoitu oliiviöljy on neutraalia.
Kaikkinensa omega-6 ja -3 rasvahappojen tulehdustarina on hyvä osoitus siitä, että pelkkään biokemian kirjaan tai koeputki- ja koe-eläintöihin nojaamalla ei voi tehdä luotettavia päätelmiä siitä, miten ravitsemus vaikuttaa ihmisessä.
Tulehduksen kannalta hyvä ruokavalio sisältää runsaasti omega-3 rasvahappoja sekä kalasta että kasviöljyistä tai pähkinöistä sekä vähäisesti tai kohtuullisesti tyydyttynyttä rasvaa. Tulehduksen kannalta huono ruokavalio on sellainen jossa vieroksutaan rasvaista kalaa, kasviöljyjä, margariinia ja pähkinöitä sekä painotetaan tyydyttynyttä rasvaa.
PS. Koska rasva ei ole kaikki kaikessa, seuraavassa osassa (3) aiheena ovat hiilihydraatit
PS2. Tästä kirjoituksesta löytyy lyhennetty ja kuvitettu versio täältä.
Keskeiset lähteet (loput linkkeinä tekstissä)
Calder Philip. Polyunsaturated fatty acids and inflammatory processes: New twists in an old tale. Biochimie 2009;91:791–795
Tässä katsauksessa rasvojen aiheuttamiin tulehdusvaikutuksiin perehtynyt Calder esittää useita teesejä ja niille todisteita, joiden perusteella voidaan sanoa, että vanha rasvaoppi omegojen inflammaatiovaikutuksista on aikansa elänyt.
Fitó et al. Anti-inflammatory effect of virgin olive oil in stable coronary disease patients: a randomized, crossover, controlled trial. Eur J Clin Nutr. 2008 Apr;62(4):570-4
Tässä harvinaislaatuisessa tutkimuksessa voitiin osoittaa, että extra virgin oliiviöljy vähentää tulehdusarvoja paastossa (CRP ja IL-6) kun taas raffinoitu oliiviöljy on neutraali. Tutkimus kesti kolme viikkoa ja oliiviöljyn annos oli suuri, 50 g/pv.
Harte et al. High fat intake leads to acute postprandial exposure to circulating endotoxin in type 2 diabetic subjects. Diabetes Care. 2012 ;35(2):375-82
Tämän tutkimuksen mukaan suuri kerta-annos tyydyttynyttä rasvaa lisää suoliston bakteereista vapautuvan LPS:n määrää veressä. LPS aiheuttaa tulehdusvasteita laajasti eri puolilla elimistöä ja on ns. endotoksiini. Tyydyttynyt rasva lisää LPS:n määrää verenkierrossa erityisen paljon diabeetikoilla.
Johnson & Fritsche. Effect of Dietary Linoleic Acid on Markers of Inflammation in Healthy Persons: A Systematic Review of Randomized Controlled Trials. Journal of the Academy of Nutrition and Dietetics 2012; 112: 1029-1041
Tämä meta-analyysi käsitti 15 tutkimusta, joista 14 osoitti linolihapon (omega-6 rasvahappo) saannilla olevan neutraali vaikutus elimistön tulehdustilaan erilaisilla tulehdusmarkkereille mitattuna. Vain yhdessä tutkimuksessa virtsaan erittyvissä metaboliiteissa havaittin eroja. Vertailurasvoina oli sekalaisia rasvoja kuten tyydyttynyttä rasvaa, oliiviöljyä jne. Meta-analyysissä on mukana useita Viikistä lähtöisin olevien ravitsemustutkijoiden tuloksia. Käytetyt linolihappoannokset olivat keskimäärin 20-30 grammaa /pv linolihappojakson aikana (enimillään 50 g/pv) ja kontrolliruokavalioissa 0-5 g (enimillään 10 g/pv). Suomalaisten linolihapon saanti on nykyisin n. 10 grammaa per päivä suomalaisten suosiessa rypsiöljyä.
Rangel-Huerta et al. Omega-3 long-chain polyunsaturated fatty acids supplementation on inflammatory biomakers: a systematic review of randomised clinical trials. Br J Nutr. 2012;107 Suppl 2:S159-70
Tämän meta-analyysin mukaan 26 tutkimusta kattaneen meta-analyysin mukaan omega-3 rasvahapoilla on merkitystä tulehduksen vähentämisessä erityisesti jo sairastuneilla (sydän- ja munuaistaudit). Sen sijaan terveillä tehdyissä kuudessa tutkimuksessa omega-3 rasvahapposupplementaatio ei yhdessäkään vaikuttanut merkittävästi tulehdusarvoihin. Rasittavan urheilun jälkeen kalaöljy saattaa vähentää tulehdusta.
Rett & Whelan. Increasing dietary linoleic acid does not increase tissue arachidonic acid content in adults consuming Western-type diets: a systematic review. Nutr Metab (Lond). 2011 Jun 10;8:36.
Meta-analyysi vuodelta 2011, joka kattoi 36 kliinistä tutkimusta. Meta-analyysin mukaan linolihapon vähentäminen 10 %:iin tavanomaisesta tai lisääminen kolminkertaiseksi tavanomaiseen verrattuna ei vaikuta ihmisessä arakidonihapon pitoisuuksiin. Tämä meta-analyysi on kuin jyrä kaikkia koeputki- ja koe-eläintöihin perustuvia teorioita ja väitteitä vastaan, joiden mukaan linolihappo on pahasti tulehdusta edistävä.
Reijo Laatikainen, rasvakirjoitusten yhteenveto
Tässä yhteenvedossa totean aiempiin kirjallisuuskatsauksiin ja erityisesti varhaisiin rasvoilla tehtyihin kuolleisuus- ja sairastuvuus tutkimuksiin perustuen, että edes jyrkkä rasvan saannin muuttaminen ei vaikuta yksiselitteisesti ja radikaalisti sydäninfarktien ja kuolemien ilmaantumiseen, ei suuntaan-ei toiseen. Jos jotakin, niin linolihappopainotteinen ruokavalio vähentää sydäntapahtumia n. 15 % useiden vuosien seurannassa vs tyydyttyneeseen rasvaan painottuva ruokavalio. Siten rasvan laadun merkitystä terveydelle ei pidä liioitella, edes tulehduksen näkökulmasta.
Tholstrup et al. Dietary cocoa butter or refined olive oil does not alter postprandial hsCRP and IL-6 concentrations in healthy women. Lipids. 2011;46(4):365-70
Tässä tutkimuksessa osoitettiin, että raffinoitu oliiviöljy suurella annoksella (1 g/kg, keskimäärin 62 g/kerta) ei aiheuta rasvarasituskokeessa CRP tai IL-6 vastetta. Tämä on vastakkainen havainto tyydyttyneelle rasvalle.
Warensjö et al. Effects of saturated and unsaturated fatty acids on estimated desaturase activities during a controlled dietary intervention. Nutr Metab Cardiovasc Dis. 2008;18(10):683-90
Tämän ihmisillä tehdyn tutkimuksen mukaan tyydyttynyt rasva estää ALA:n muuttumista EPA:ksi ja lisää linolihapon muuttumista arakidonihapoksi. Das on aiemmin osoittanut koe-eläimillä saman periaatteen todeksi ALA:n osalta.